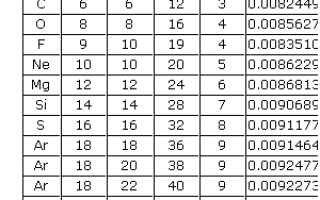
В статье рассмотрим атомные массы некоторых изотопов и концепцию насыщения ядерных сил. Понимание атомных масс и изотопов важно для ядерной физики, химии и медицины. Эти характеристики помогают глубже понять структуру атома и применять знания в радиотерапии, радиохимии и исследовании ядерных реакций.
Энергия связи ядра — материалы для подготовки к ЕГЭ по Физике
Такое внимание к деталям необходимо для вычисления ключевой величины, часто используемой в расчетах ядерной энергии и реакций.
Согласно нуклонной модели, атомное ядро состоит из нуклонов — протонов и нейтронов. Но что удерживает нуклоны вместе внутри ядра?
Предположим, два протона находятся на определенном расстоянии друг от друга. Мы можем определить соотношение между силой их электрического отталкивания и силой гравитационного притяжения:
Электрическая сила значительно превосходит гравитационное притяжение. Оно не обеспечивает стабильность ядра и практически незаметно по сравнению с электрическим отталкиванием.
Таким образом, существуют другие силы, которые притягивают нуклоны и превосходят электрическое отталкивание протонов. Эти силы известны как ядерные силы.
- Эти силы действуют между частицами независимо от наличия электрического заряда, то есть как между протонами, так и между нейтронами, а также между протонами и нейтронами. Это явление называется зарядовой независимостью ядерных сил.
- Ядерные силы являются сильнодействующими; по величине они на порядок превышают любые другие известные силы в природе (гравитационные, электрические, магнитные и т. д.), включая электростатическое отталкивание между протонами в ядре.
- Ядерные силы — короткодействующие, они проявляют действие только на малых расстояниях, сопоставимых с размерами ядра (порядка 10^-12 — 10^-13 см), и с увеличением расстояния их влияние быстро ослабевает (обратно пропорционально седьмой степени расстояния).
Эксперты в области ядерной физики подчеркивают важность точного определения атомных масс изотопов для понимания ядерных взаимодействий и их свойств. Насыщение ядерных сил, как отмечают ученые, играет ключевую роль в стабильности атомных ядер и их реакциях. Исследования показывают, что атомные массы изотопов могут варьироваться в зависимости от их ядерной структуры и взаимодействий между нуклонами. Это, в свою очередь, влияет на такие процессы, как радиоактивный распад и ядерные реакции. Ученые акцентируют внимание на необходимости постоянного обновления таблиц атомных масс, чтобы обеспечить точность в расчетах и моделировании ядерных процессов. Важно отметить, что понимание насыщения ядерных сил может привести к новым открытиям в области ядерной энергетики и медицины.

Глава 2. Разбор задач
Определить, какую часть массы нейтрального атома Pu-240 составляет масса его электронной оболочки относительную атомную массу принять равной массовому числу.
| Изотоп | Атомная масса (а.е.м.) | Энергия связи на нуклон (МэВ) |
|---|---|---|
| ¹H | 1.007825 | 0 |
| ²H | 2.014102 | 1.11 |
| ³H | 3.016050 | 2.83 |
| ⁴He | 4.002603 | 7.07 |
| ¹²C | 12.000000 | 7.68 |
| ¹⁴N | 14.003074 | 7.47 |
| ¹⁶O | 15.994915 | 7.98 |
| ²³⁵U | 235.0439299 | 7.59 |
| ²³⁸U | 238.0507882 | 7.57 |
Интересные факты
Вот несколько интересных фактов, связанных с атомными массами изотопов и насыщением ядерных сил:
-
Изотопы и их стабильность: Атомные массы изотопов одного и того же элемента могут значительно различаться, что связано с количеством нейтронов в ядре. Например, углерод имеет три стабильных изотопа: углерод-12 (с 6 нейтронами), углерод-13 (с 7 нейтронами) и углерод-14 (с 8 нейтронами). Углерод-14 является радиоактивным и используется в радиоуглеродном датировании, что позволяет определять возраст органических материалов.
-
Насыщение ядерных сил: Ядерные силы, отвечающие за связывание нуклонов (протонов и нейтронов) в ядре, демонстрируют эффект насыщения. Это означает, что при добавлении дополнительных нуклонов в ядро, сила взаимодействия не увеличивается пропорционально количеству нуклонов. Например, в тяжелых ядрах, таких как уран, добавление дополнительных нейтронов может привести к нестабильности и радиоактивному распаду.
-
Массовый дефект и энергия связи: Массовый дефект — это разница между суммарной массой нуклонов, составляющих ядро, и фактической массой самого ядра. Эта разница объясняется тем, что часть массы превращается в энергию связи, удерживающую нуклоны вместе. Чем больше масса дефекта, тем больше энергия связи, что делает ядро более стабильным. Это явление лежит в основе ядерной энергии и реакций деления и слияния.

Что такое строение ядра атома
Количество протонов в ядре соответствует порядковому номеру элемента в периодической таблице, известному как атомный номер или зарядовое число Z.
Общее количество нуклонов — сумма протонов и нейтронов — определяет атомный вес элемента, округленный до целых значений, и называется массовым числом A.
Ядро обозначается химическим символом элемента с указанием атомного номера и массового числа в виде индексов, например:
Пример обозначения
Соответственно обозначаются и ядерные частицы: протон — 1p 1 и нейтрон —0n 1 . На рис. 1 изображены схематически ядра водорода, гелия, лития, азота и алюминия (на рис. 1, так же как и на последующих, протоны изображаются черными кружками, нейтроны — белыми).
Предполагается, что они имеют обменную природу, т. е. возникают в процессе непрерывного обмена между нуклонами особыми частицами (квантами ядерного поля), которые называются π-мезонами.

Изотопы
Существуют атомы с одинаковым атомным номером, но различным массовым числом.
1851. Определите количество электронов в атоме брома ^Br. Каков суммарный заряд всех электронов в элементарных зарядах e?
1864. Ядро атома криптона ^Kr шесть раз подверглось бета-распаду. Какое ядро образуется? Запишите уравнения реакций.
1865. Ядро атома ксенона ^Xe превращается в стабильное ядро атома церия ^Ce. Сколько электронов выделяется? Запишите уравнения этих реакций.
1866. Как изменяется массовое число элемента при испускании гамма-кванта? Изменяются ли масса ядра и порядковый номер элемента?
1867. Альфа-частица испускается ядром, образовавшимся в результате бомбардировки изотопа бора ^B нейтронами. В какой элемент превратился изотоп бора ^B? Запишите эту реакцию.
1868. При облучении плутония ^Pu ядрами неона ^Ne образуется элемент резерфордий и четыре нейтрона. Напишите уравнение реакции.
1869. Допишите недостающие символы X, Z, A в ядерных реакциях:
а) ^1H + ^X → ^4He + ^1n;
б) ^X + ^1H → ^32He + ^11e;
в) ^U + ^X → ^Es + ^8n
1870. Масса атома бора составляет 11,009305 а.е.м., масса атома водорода — 1,007825 а.е.м., масса нейтрона — 1,008665 а.е.м. Определите дефект массы ядра бора ^B. Какова энергия связи ядра бора?
Влияние изотопов на стабильность ядер
Изотопы являются разновидностями одного и того же химического элемента, которые имеют одинаковое количество протонов, но различное количество нейтронов в ядре. Это различие в нейтронном составе приводит к изменению атомной массы изотопов, что, в свою очередь, влияет на их стабильность и поведение в ядерных реакциях. Стабильные изотопы имеют ядра, которые не подвергаются радиоактивному распаду, тогда как нестабильные изотопы распадаются с течением времени, испуская радиацию.
Стабильность ядер изотопов определяется балансом между силами, действующими внутри ядра. Ядерные силы, которые связывают протоны и нейтроны, действуют на очень коротких расстояниях и являются сильными, но они должны преодолевать отталкивание между положительно заряженными протонами. В этом контексте количество нейтронов в ядре играет ключевую роль: нейтроны помогают уменьшить отталкивание между протонами, обеспечивая дополнительную силу связи.
С увеличением числа протонов в ядре (то есть с увеличением атомного номера) требуется больше нейтронов для поддержания стабильности. Это связано с тем, что отталкивание между протонами возрастает, и для его компенсации необходимо больше нейтронов. Например, углерод-12 (с 6 протонами и 6 нейтронами) является стабильным изотопом, тогда как углерод-14 (с 6 протонами и 8 нейтронами) является радиоактивным и распадается с течением времени.
Некоторые изотопы могут быть стабильными в определенных условиях, но нестабильными в других. Например, изотопы с большим количеством нейтронов могут быть стабильными при низких энергиях, но могут стать нестабильными при высоких энергиях или в условиях высокой плотности. Это явление наблюдается в звездах, где высокие температуры и давления могут приводить к образованию нестабильных изотопов.
Изучение изотопов и их влияния на стабильность ядер имеет важное значение для различных областей науки, включая ядерную физику, астрофизику и радиобиологию. Понимание того, как изотопы взаимодействуют и как они влияют на стабильность ядер, помогает ученым разрабатывать новые технологии, такие как ядерные реакторы, медицинские приложения радионуклидов и методы датирования.
В заключение, влияние изотопов на стабильность ядер является сложным и многогранным процессом, который зависит от соотношения протонов и нейтронов, а также от условий, в которых эти ядра находятся. Исследование этих аспектов продолжает оставаться актуальным и важным для дальнейшего понимания ядерной физики и ее приложений.
Вопрос-ответ
Что такое насыщение ядерных сил?
Ядерные силы обладают свойством насыщения. Это проявляется в том, что нуклон в ядре взаимодействует лишь с ограниченным числом ближайших к нему в ядре соседних нуклонов. Следствием свойства насыщения является линейная зависимость энергии связи ядер от их массового числа A.
Как измеряют массы атомных ядер?
В качестве единицы измерения атомных и молекулярных масс принята 1/12 часть массы нейтрального атома наиболее распространённого изотопа углерода 12C. Эта внесистемная единица измерения массы получила название атомная единица массы (а. е. м.).
Чему равна атомная масса ядра?
Масса ядра равна сумме масс протонов и нейтронов. Число протонов определяем по порядковому номеру элемента. Значит, число нейтронов в ядре можно найти, если от относительной атомной массы отнять порядковый номер.
Какова формула массы ядра?
Eсв(A, Z) = [Zmp + (A – Z)mn – M(A, Z)]c2.
Советы
СОВЕТ №1
Изучите основные принципы ядерной физики, чтобы лучше понять, как атомные массы изотопов влияют на их стабильность и поведение. Это поможет вам глубже осознать значение насыщения ядерных сил.
СОВЕТ №2
Обратите внимание на таблицы атомных масс изотопов, так как они содержат важную информацию о соотношении между различными изотопами и их ядерными свойствами. Сравнение этих данных может дать вам полезные инсайты.
СОВЕТ №3
Используйте визуальные материалы, такие как графики и схемы, чтобы лучше воспринимать информацию о насыщении ядерных сил. Визуализация может значительно облегчить понимание сложных концепций.
СОВЕТ №4
Не забывайте о практических приложениях изучаемых тем. Исследуйте, как атомные массы и насыщение ядерных сил применяются в ядерной энергетике, медицине и других областях, чтобы увидеть реальное значение этих знаний.